Tehnologiile de identificare unică a dispozitivelor automatizează citirea ID-urilor medicale și a codurilor de bare
Contributed By DigiKey's North American Editors
2023-10-26
În 2013, Administrația pentru Alimente și Medicamente (FDA) din SUA a implementat sistemul de identificare unică a dispozitivelor sau regula UDI. Regula urmărea să îmbunătățească siguranța pacienților prin furnizarea unei metode consecvente de urmărire și identificare a dispozitivelor medicale prin utilizarea unei documentări moderne la punctele de fabricație, distribuție și utilizare. La fel ca și cerințele reglementărilor privind dispozitivele medicale din Europa sau ca și reglementările similare din alte țări, regula UDI din SUA sporește acuratețea raportării și facilitează analiza în cazul unei retrageri sau al unui eveniment advers.
Începând cu 24 septembrie 2023, FDA va aplica integral Numerele naționale de cod pentru articole medicale și pentru medicamente pe etichetele și ambalajele dispozitivelor. Toate produsele medicale etichetate la această dată sau după această dată trebuie să respecte pe deplin mandatele UDI. Acest mandat va afecta următoarele:
- Produsele din clasa 3, esențiale pentru viață, cum ar fi stimulatoarele cardiace și protezele implantate
- Produsele din clasa 2, moderat critice, cum ar fi seringi, catetere și suturi absorbabile
- Produsele din clasa 1 cu risc redus, cum ar fi ața dentară, halate medicale și măști de oxigen
Punerea în aplicare integrală a mandatului înseamnă că, dacă un dispozitiv medical nu are un cod de bare scanabil, acesta nu va mai fi considerat un produs valabil/utilizabil, chiar dacă pe el există etichete ce pot fi citite de oameni și chiar dacă se presupune în general că produsul este ușor de identificat de către majoritatea utilizatorilor. Această implementare integrală va stimula o adoptare cuprinzătoare de către industria medicală și facturarea asigurărilor medicale.
 Figura 1: Unele verificatoare portabile de coduri de bare marcate direct pe piesă (DPM) dispun de iluminare avansată și de alte programe software pentru a găsi automat simbolurile și pentru a parcurge setările pentru a optimiza citirea mărcii DPM specifice și a respectivului substrat de material. De fapt, LVS-9585 prezentat aici poate verifica atât piesele DPM, cât și etichetele tipărite, pentru o analiză și raportare cuprinzătoare. (Sursa imaginii: Omron Automation)
Figura 1: Unele verificatoare portabile de coduri de bare marcate direct pe piesă (DPM) dispun de iluminare avansată și de alte programe software pentru a găsi automat simbolurile și pentru a parcurge setările pentru a optimiza citirea mărcii DPM specifice și a respectivului substrat de material. De fapt, LVS-9585 prezentat aici poate verifica atât piesele DPM, cât și etichetele tipărite, pentru o analiză și raportare cuprinzătoare. (Sursa imaginii: Omron Automation)
Entitatea contractantă (purtătorul mărcii) poartă responsabilitatea
În Statele Unite, deținătorul proprietății intelectuale și brandul care se adresează utilizatorului pentru fiecare produs medical este responsabil pentru acuratețea și calitatea codurilor UDI. Acest lucru este deosebit de important, deoarece o mare parte din piața produselor medicale este fabricată pe bază de contracte și externalizată în unitățile altor organizații. Prin urmare, organizația contractantă are responsabilitatea de a se asigura că întregul său lanț de aprovizionare este conform cu UDI și că produce etichete corecte.
Originile tehnologiei de identificare unică a dispozitivelor
UDI-urile sunt identificatori statici de dispozitive. Cu toate acestea, modificarea cantității de articole dintr-un pachet poate determina necesitatea unui nou identificator. Agențiile emitente dictează modul în care se disting aceste detalii. În același mod, și modificarea condițiilor de sterilitate a ambalajului unui dispozitiv poate modifica identificatorul dispozitivului. Schimbarea pieței de destinație a unui dispozitiv (țara în care un dispozitiv va fi vândut), a limbii de pe etichetă sau a mărcii CE poate necesita, de asemenea, modificări ale identificatorului dispozitivului.
Înainte de regula UDI, un producător de dispozitive medicale putea să eticheteze un produs cu un anumit număr de piesă. Distribuitorul schimba acel număr de piesă înainte ca furnizorul de servicii medicale sau spitalul să îl schimbe din nou. Având în vedere posibilitatea ca fiecare entitate să schimbe numărul piesei înainte ca aceasta să ajungă la pacient, era aproape imposibil să se urmărească produsele, să se gestioneze retragerile, să se prevină contrafacerea sau să se comande cu precizie și eficiență stocuri noi.
Conținut asociat: Implementarea unor soluții robuste de trasabilitate
În prezent, fiecărui dispozitiv i se atribuie un identificator standardizat și persistent, numit UDI, pentru a permite tuturor entităților o identificare mai rapidă și mai precisă a dispozitivului, reducând în cele din urmă erorile medicale. Acest UDI este un cod alfanumeric care conține două date esențiale:
- Un identificator de dispozitiv
- Un identificator de producție
Un identificator de dispozitiv este o etichetă statică atribuită unui anumit dispozitiv, pe care sunt trecute numele celui care l-a etichetat (de obicei, producătorul dispozitivului) și numărul de model specific al dispozitivului. În schimb, un identificator de producție conține date care pot varia, iar o mare parte din datele pe care le poate conține sunt opționale. Acestea pot include coduri de lot de producție și lot de ambalare, numere de serie, date de expirare și date de fabricație. Pe scurt, datele opționale ar putea fi orice lucru pe care un producător sau un etichetator îl consideră necesar pentru a susține urmărirea dispozitivului.
Fiecare etichetă UDI trebuie să prezinte aceste informații în două forme:
- Formă lizibilă pentru om (text simplu)
- Formă lizibilă pentru dispozitive (care poate fi citită de un cititor de coduri de bare sau RFID)
În cazul în care un dispozitiv poate fi utilizat pentru mai multe aplicații medicale, UDI trebuie să fie marcat direct pe dispozitiv, nu pe ambalaj. Regula se aplică, de asemenea, dispozitivelor care pot fi utilizate de mai multe ori.
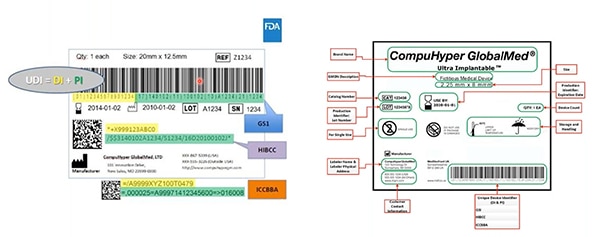 Figura 2: GS1, HIBCC și ICCBBA – agențiile emitente de UDI – creează UDI-uri; atribuie simbolistica permisă pentru UDI; definesc ce tehnologii pot interfața cu UDI-urile; și specifică calitatea necesară a mărcilor UDI. Pe acest eșantion este evidențiat cu galben identificatorul dispozitivului; cu verde sunt evidențiați identificatorii de producție. Alte elemente includ informații care pot fi citite de către om ... și care sunt, de asemenea, integrate în codul de bare care poate fi citit de către dispozitive. (Sursa imaginii: FDA)
Figura 2: GS1, HIBCC și ICCBBA – agențiile emitente de UDI – creează UDI-uri; atribuie simbolistica permisă pentru UDI; definesc ce tehnologii pot interfața cu UDI-urile; și specifică calitatea necesară a mărcilor UDI. Pe acest eșantion este evidențiat cu galben identificatorul dispozitivului; cu verde sunt evidențiați identificatorii de producție. Alte elemente includ informații care pot fi citite de către om ... și care sunt, de asemenea, integrate în codul de bare care poate fi citit de către dispozitive. (Sursa imaginii: FDA)
Toate dispozitivele trebuie să fie înregistrate în baza de date globală UDI pentru a permite urmărirea în cazul unei retrageri și pentru a oferi publicului acces la informații despre un anumit dispozitiv. Agențiile emitente acreditate de FDA sunt autorizate să creeze identificatori unici pe care producătorii de dispozitive să îi aplice pe produsele lor.
Carte albă conexă: Cum să rămâneți la curent cu cerințele privind trasabilitatea
Tehnologii și tehnici de scanare UDI
Etichetele UDI pot fi verificate în mai multe moduri de-a lungul traseului lor de la fabricare la utilizare.
Verificarea în linie este realizată prin tehnologii integrate în utilaje mai mari pentru procesarea rapidă și precisă a unui număr mare de produse pe măsură ce acestea sunt fabricate. Sprijinite de un software avansat, aceste tehnologii iau uneori forma unor imprimante de etichete de nivel industrial. Aceste imprimante sunt capabile să efectueze propria verificare în linie pentru a confirma că informațiile UDI sunt lizibile conform standardelor stricte ale industriei imediat după crearea lor la punctul de producție a etichetei. De exemplu, verificatoarele V275 de la Omron Automation pot fi utilizate cu imprimantele termice Zebra pentru a îndeplini cerințele standardelor ISO 15426 și ale standardelor GS1 ale autorității emitente pentru conformitatea cu FDA.
Conținut asociat: Soluții de trasabilitate Omron
Pe de altă parte, verificarea în linie ia forma unor sisteme specializate de vedere artificială care însoțesc benzile transportoare pe liniile de producție automatizate, încorporând citirea codurilor de bare pentru o verificare extrem de rapidă și precisă a etichetării UDI pe produse cu un grad ridicat de combinații pe liniile de producție de mare viteză. Ofertele MicroHAWK de la Omron Automation excelează în acest domeniu, cu senzori avansați, completați de o construcție miniaturizată și opțiuni de conectivitate care includ Ethernet/IP și PROFINET.
Conținut asociat: Scăpați de responsabilitatea pentru etichetarea necorespunzătoare
În schimb, verificarea UDI offline este cea mai potrivită pentru eșantionarea loturilor de etichete pentru a asigura calitatea. Adesea utilizată pentru testarea eșantioanelor atunci când dispozitivele medicale părăsesc sau sosesc la o unitate, verificarea offline poate completa sistemele de verificare online din amonte, pe parcursul procesului de distribuție.
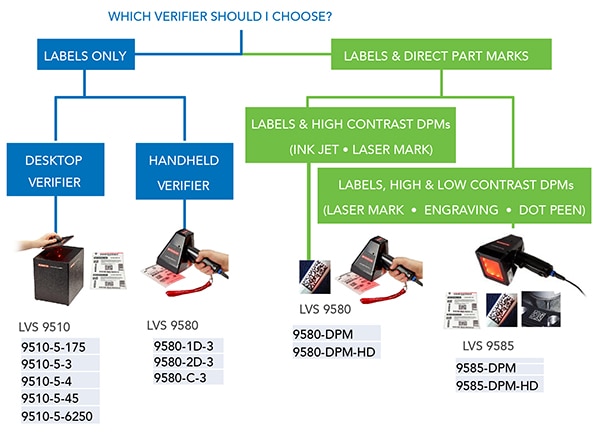 Figura 3: UDI-urile marcate direct pe produse necesită verificatori diferiți de cei utilizați pentru UDI-urile imprimate pe etichete aplicate. (Sursa imaginii: Omron Automation)
Figura 3: UDI-urile marcate direct pe produse necesită verificatori diferiți de cei utilizați pentru UDI-urile imprimate pe etichete aplicate. (Sursa imaginii: Omron Automation)
De fapt, toate operațiunile de distribuție de produse medicale și de asistență medicală pot beneficia de utilizarea verificatoarelor conforme cu ISO. Luați ca exemplu produsele din seria LVS 95XX de la Omron pentru verificarea offline a UDI. Acestea sunt utilizate:
- La stațiile de marcare cu laser și la imprimantele de etichete unde sunt create coduri
- În zonele în care codurile sunt aplicate pe produse, care pot fi sau nu separate de zona de creare a codului
- În stațiile de control al calității, unde sunt confirmate șabloanele, formatarea și alte elemente de cod
Specificarea variațiilor verificatorului UDI offline
Cel mai potrivit verificator UDI offline pentru o anumită aplicație depinde de mai mulți parametri.
Dimensiunea codului de bare: Codurile de bare de mari dimensiuni sunt adesea mai ușor de scanat cu ajutorul identificatorilor care au un câmp vizual larg, definit de distanța focală a obiectivului și de dimensiunea senzorului. Luați ca exemplu identificatorii UDI desktop LVS-9510 de la Omron Automation. Această serie de produse poate citi atât etichete liniare, cât și 2D. Cinci versiuni diferite oferă câmpuri de vizualizare diferite, astfel ca proiectanții să poată selecta versiunea compatibilă cu dimensiunea codului de bare care trebuie verificat. O funcție de combinare permite clasificarea codurilor de bare care depășesc câmpul de vizualizare.
În plus, toate dispozitivele LVS-9510 pot determina automat simbologia și diafragma necesare pentru a evalua codul și pentru a identifica și evidenția punctele cu probleme.
 Figura 4: Verificarea codurilor de bare care respectă standardele ISO este mai ușoară cu ajutorul echipamentelor care pot verifica atât codurile liniare (1D), cât și cele bidimensionale (2D). Unele astfel de echipamente determină simbologia și diafragma necesare pentru a evalua codurile și identifică și evidențiază problemele. Modelul LVS-9510 prezentat aici are o funcție de combinare care permite clasificarea codurilor de bare mai mari decât câmpul de vizualizare. (Sursa imaginii: Omron Automation)
Figura 4: Verificarea codurilor de bare care respectă standardele ISO este mai ușoară cu ajutorul echipamentelor care pot verifica atât codurile liniare (1D), cât și cele bidimensionale (2D). Unele astfel de echipamente determină simbologia și diafragma necesare pentru a evalua codurile și identifică și evidențiază problemele. Modelul LVS-9510 prezentat aici are o funcție de combinare care permite clasificarea codurilor de bare mai mari decât câmpul de vizualizare. (Sursa imaginii: Omron Automation)
Tipul codului de bare: Scanerele trebuie să citească formatele de coduri de bare atribuite de organismele emitente cunoscute sub numele de HIBCC, ICCBBA sau (cel mai frecvent începând cu 2023) GS1. GS1 dictează dimensiunea, formatul și rezoluția codurilor UPC, a codurilor de bare liniare și a codurilor de bare cu matrice de date 2D.
Amplasarea mărcii UDI: Luați ca exemplu marcarea directă a pieselor (DPM) pentru dispozitivele medicale. Aceste marcaje pot fi incredibil de mici, în special atunci când identifică instrumente chirurgicale și dispozitive medicale implantabile. Pentru a citi și a verifica astfel de UDI-uri DPM, verificatoarele portabile de foarte mare densitate LVS-9580 și LVS-9585 de la Omron dispun de o lentilă specializată care poate citi o multitudine de DPM-uri, inclusiv cele cu dimensiuni ale celulelor de până la 0,0508 mm (0,002 in). Lentilele de calitate industrială din interiorul LVS-9580 și LVS-9585 asigură o precizie de citire constantă. Cele mai sofisticate sunt tehnologiile cu iluminare extrem de controlabile și calibrabile din interiorul scanerelor. Alături de câmpurile multiple de vizualizare, iluminarea permite optimizarea imediată a imaginilor UDI capturate. Acest lucru este deosebit de important, deoarece standardul privind codurile nu permite corecții sau manipulări ulterioare ale imaginii.
Mai multe despre software-ul de scanare UDI
Pentru eficacitate maximă, software-ul UDI pentru susținerea hardware-ului verificatorului trebuie să prezinte informațiile de diagnosticare într-un format intuitiv. Acest software trebuie să clasifice codurile UDI în conformitate cu parametrii definiți de ISO (cel mai important fiind confirmarea lizibilității acestora) și, în mod ideal, ar trebui să urmărească și problemele legate de degradare pe parcursul unei serii de scanări UDI.
Omron include tot software-ul necesar cu fiecare dintre echipamentele sale de scanare UDI. Software-ul este actualizat în mod regulat pentru a ține pasul cu evoluția rapidă a reglementărilor și cu noua legislație din domeniu.
O funcție majoră a software-ului de scanare Omron este manipularea sintaxei codurilor. Pe scurt, fiecare cod de bare sau cod 2D trebuie să extragă cu exactitate toate informațiile pertinente, inclusiv tipul de produs, numărul de lot, cantitatea, după caz, data de expirare, informațiile de expediere etc. Șirurile de date rezultate trebuie să fie formatate într-un mod special pentru a ține pasul cu cerințele, metodologiile și destinațiile produselor medicale aflate mereu în evoluție.
Software-ul actualizat în mod regulat de către producătorul scanerului asigură faptul că utilizatorii finali rămân la curent chiar și atunci când se lansează coduri noi.
Concluzie
Armata americană a avut cândva ca obiectiv să utilizeze pe deplin un sistem de urmărire a produselor UID, precum sistemul UDI din industria medicală. Scopul acestuia era de a reduce risipa masivă asociată cu pierderile, duplicările și stocurile necontorizate din instalațiile militare, inclusiv orice, de la armament Raytheon finalizat până la panouri de control furnizate de o mică unitate pentru o aplicație specializată. În prezent, UID-urile sunt utilizate în diferite moduri.
Mandatul UDI nu va avea aceeași soartă.
Conceptul care determină adoptarea UDI este simplu: Eticheta este produsul. La urma urmei, o etichetă incorectă poate cauza un lanț de evenimente care irosește timpul personalului medical și duce la aruncarea dispozitivului medical. Așadar, UDI-urile trebuie să apară pe toate straturile ambalajelor, cum ar fi pe unitate, ambalaj, pachet, ladă, cutie și palet. UDI-urile de pe dispozitivele medicale sterile aflate în interiorul sigiliilor sterile sunt deosebit de importante, deoarece ruperea sigiliului pentru a verifica tipul de dispozitiv este inacceptabilă.
Având în vedere că FDA solicită respectarea deplină a directivelor UDI începând cu 24 septembrie 2023, tehnologiile avansate de scanare pentru verificarea produselor medicale vor deveni esențiale pentru producătorii de automatizări, precum și pentru constructorii de utilaje și utilizatorii finali pe care îi deservesc.
Astfel de scanere pot îndeplini cerințele extrem de specifice ale UDI FDA pentru a confirma etichetele de pe o gamă largă de echipamente de laborator, medicale și de diagnosticare clinică. Verificatoarele de coduri de bare offline maximizează trasabilitatea, vederea artificială în linie și cititoarele DPM avansate.

Disclaimer: The opinions, beliefs, and viewpoints expressed by the various authors and/or forum participants on this website do not necessarily reflect the opinions, beliefs, and viewpoints of DigiKey or official policies of DigiKey.






